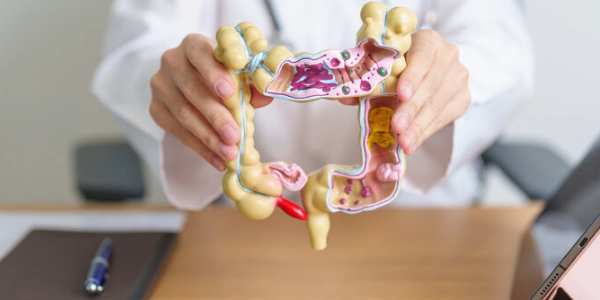
Darmkrebs ist weltweit die zweithäufigste Ursache für krebsbedingte Todesfälle. Bei frühzeitiger Erkennung ist er oft sehr gut behandelbar. Koloskopien – die heute gängigste Vorsorgeuntersuchung – können jedoch kostspielig und unangenehm sein, was viele Menschen davon abhält, sich rechtzeitig untersuchen zu lassen. Forscher der Universität Genf (UNIGE) haben einen neuen Ansatz entwickelt, der dies ändern könnte. Mithilfe von maschinellem Lernen erstellten sie den ersten detaillierten Katalog aller menschlichen Darmbakterien, der so präzise ist, dass er Aufschluss darüber gibt, wie verschiedene mikrobielle Untergruppen im Körper funktionieren. Diese Informationen nutzten sie dann, um Darmkrebs anhand von Bakterien in einfachen Stuhlproben zu erkennen, und bieten damit eine nicht-invasive und kostengünstige Alternative. Die in Cell Host & Microbe veröffentlichten Ergebnisse könnten Wissenschaftlern zudem helfen, besser zu verstehen, wie die Darmmikrobiota die allgemeine Gesundheit und Krankheiten beeinflusst.
Darmkrebs: Warum bessere Vorsorgeinstrumente benötigt werden
Darmkrebs ist eine bösartige Tumorerkrankung des Dick- oder Enddarms. In den meisten Fällen entwickelt er sich langsam aus zunächst gutartigen Wucherungen der Darmschleimhaut, sogenannten Polypen, die sich über Jahre hinweg verändern können. Gerade weil dieser Prozess oft lange unbemerkt bleibt, spielt Früherkennung eine entscheidende Rolle.

Das Risiko steigt vor allem mit dem Alter deutlich an – die meisten Erkrankungen treten ab etwa 50 Jahren auf. Weitere Risikofaktoren sind eine familiäre Vorbelastung, Übergewicht, Bewegungsmangel, eine ballaststoffarme Ernährung sowie hoher Konsum von rotem oder verarbeitetem Fleisch und Alkohol. Darmkrebs gehört zu den häufigsten Krebsarten in Europa, sowohl bei Männern als auch bei Frauen, wobei die Erkrankung bei Männern etwas häufiger vorkommt.
Typische Symptome treten oft erst in fortgeschrittenen Stadien auf. Dazu gehören Veränderungen der Stuhlgewohnheiten (z. B. anhaltender Durchfall oder Verstopfung), Blut im Stuhl, unklare Bauchschmerzen, Gewichtsverlust oder anhaltende Müdigkeit durch Blutarmut. Da diese Anzeichen unspezifisch sein können, ist es besonders wichtig, Vorsorgeuntersuchungen wahrzunehmen – denn früh erkannt, sind die Heilungschancen in der Regel sehr gut.
Viele Fälle von Darmkrebs werden erst spät diagnostiziert, wenn die Behandlungsmöglichkeiten bereits eingeschränkt sind. Dies unterstreicht den dringenden Bedarf an einfacheren und weniger invasiven Vorsorgeverfahren, zumal die Zahl der Fälle bei jüngeren Erwachsenen aus bislang ungeklärten Gründen weiter zunimmt. Wissenschaftler wissen seit langem, dass die Darmmikrobiota eine Rolle bei Darmkrebs spielt. Es war jedoch schwierig, dieses Wissen in praktische medizinische Instrumente umzusetzen. Eine große Herausforderung besteht darin, dass sich verschiedene Stämme innerhalb derselben Bakterienart sehr unterschiedlich verhalten können. Einige tragen möglicherweise zur Krebsentstehung bei, während andere keinerlei Wirkung haben.
Fokus auf Unterarten der Mikrobiota
Die Darmmikrobiota bezeichnet die Gesamtheit aller Mikroorganismen, die in unserem Darm leben. Dazu gehören vor allem Bakterien, aber auch Viren, Pilze und andere Mikroben. Jeder Mensch trägt davon Milliarden bis Billionen in sich – sie bilden ein komplexes, eigenes Ökosystem, das eng mit unserem Körper zusammenarbeitet. Diese Mikroorganismen erfüllen wichtige Funktionen: Sie helfen bei der Verdauung, produzieren bestimmte Vitamine, trainieren das Immunsystem und beeinflussen sogar Stoffwechselprozesse. Gleichzeitig stehen sie in ständigem Austausch mit dem Körper. Gerät dieses Gleichgewicht aus der Balance – etwa durch Ernährung, Medikamente oder Krankheiten – kann sich das auf die Gesundheit auswirken und mit verschiedenen Erkrankungen in Verbindung stehen.
 „Anstatt uns auf die Analyse der verschiedenen Arten zu stützen, aus denen sich die Mikrobiota zusammensetzt – was nicht alle bedeutenden Unterschiede erfasst – oder auf Bakterienstämme, die von Individuum zu Individuum stark variieren, haben wir uns auf eine Zwischenebene der Mikrobiota konzentriert, nämlich die Unterarten“, erklärte Mirko Trajkovski, ordentlicher Professor am Institut für Zellphysiologie und Stoffwechsel sowie am Diabeteszentrum der Medizinischen Fakultät der UNIGE, der diese Forschung leitete. Die Unterscheidung auf Unterartenebene ist spezifisch und kann die Unterschiede in der Funktionsweise von Bakterien und deren Beitrag zu Krankheiten wie Krebs erfassen, bleibt dabei aber allgemein genug, um diese Veränderungen zwischen verschiedenen Personengruppen, Populationen oder Ländern zu erkennen.“
„Anstatt uns auf die Analyse der verschiedenen Arten zu stützen, aus denen sich die Mikrobiota zusammensetzt – was nicht alle bedeutenden Unterschiede erfasst – oder auf Bakterienstämme, die von Individuum zu Individuum stark variieren, haben wir uns auf eine Zwischenebene der Mikrobiota konzentriert, nämlich die Unterarten“, erklärte Mirko Trajkovski, ordentlicher Professor am Institut für Zellphysiologie und Stoffwechsel sowie am Diabeteszentrum der Medizinischen Fakultät der UNIGE, der diese Forschung leitete. Die Unterscheidung auf Unterartenebene ist spezifisch und kann die Unterschiede in der Funktionsweise von Bakterien und deren Beitrag zu Krankheiten wie Krebs erfassen, bleibt dabei aber allgemein genug, um diese Veränderungen zwischen verschiedenen Personengruppen, Populationen oder Ländern zu erkennen.“
Mit maschinellem Lernen den Darm entschlüsseln
Die Forschung erforderte die Analyse riesiger Mengen biologischer Daten. „Als Bioinformatiker bestand die Herausforderung darin, einen innovativen Ansatz für die Massendatenanalyse zu entwickeln“, sagte Matija Trickovic, Doktorand in Trajkovskis Labor und Erstautor der Studie. „Wir haben erfolgreich den ersten umfassenden Katalog der Unterarten der menschlichen Darmmikrobiota entwickelt, zusammen mit einer präzisen und effizienten Methode, um ihn sowohl in der Forschung als auch in der Klinik einzusetzen.“
Die Forschenden nutzen Algorithmen, die darauf trainiert werden, in diesen riesigen Datensätzen Muster zu erkennen. Dafür füttert man das System mit vielen bereits bekannten Proben – etwa von gesunden Personen und von Patienten mit bestimmten Erkrankungen. Der Algorithmus lernt dabei, welche Kombinationen von bakteriellen Unterarten typisch für bestimmte Zustände sind, auch wenn diese Unterschiede für den Menschen kaum sichtbar wären.
Der erwähnte „Katalog“ ist dabei eine Art Referenzdatenbank: Er enthält systematisch erfasste Informationen darüber, welche mikrobiellen Unterarten im Darm vorkommen und wie sie sich unterscheiden. In Kombination mit den lernenden Algorithmen entsteht so ein Werkzeug, das neue Proben schnell einordnen kann. Das macht die Methode nicht nur für die Forschung wertvoll, sondern auch für die klinische Praxis – etwa um Krankheiten früher zu erkennen, Risiken einzuschätzen oder Therapien besser auf einzelne Personen abzustimmen.
Ein Stuhltest, der der Koloskopie in nichts nachsteht
Durch die Kombination ihres Bakterienkatalogs mit bestehenden klinischen Datensätzen entwickelte das Team ein Modell, das Darmkrebs allein anhand von Stuhlproben erkennen kann. Die Ergebnisse übertrafen die Erwartungen. „Obwohl wir von unserer Strategie überzeugt waren, waren die Ergebnisse beeindruckend“, sagte Matija Trickovic. „Unsere Methode erkannte 90 % der Krebsfälle – ein Ergebnis, das sehr nahe an der Erkennungsrate von 94 % liegt, die mit Koloskopien erreicht wird, und das besser ist als alle derzeitigen nicht-invasiven Erkennungsmethoden.“ Mit zusätzlichen klinischen Daten könnte das Modell noch genauer werden und schließlich die Leistungsfähigkeit der Koloskopie erreichen. In der Praxis könnte diese Art von Test für Routine-Screenings eingesetzt werden, wobei Koloskopien zur Bestätigung positiver Fälle vorbehalten blieben.

Der entscheidende Vorteil liegt darin, dass dieser Ansatz nicht-invasiv ist und gleichzeitig sehr viele biologische Informationen nutzt. Während klassische Stuhltests meist nur nach Blut suchen, analysiert dieses Verfahren komplexe Veränderungen im mikrobiellen Ökosystem des Darms. Dadurch kann es auch frühere oder subtilere Hinweise auf krankhafte Prozesse erkennen. In der Praxis wäre das Ziel, solche Tests breit für die Vorsorge einzusetzen und nur bei auffälligen Ergebnissen eine genauere Abklärung, etwa durch eine Darmspiegelung, folgen zu lassen.
Über die Krebserkennung hinaus
Derzeit wird in Zusammenarbeit mit den Genfer Universitätskliniken (HUG) eine klinische Studie vorbereitet, um genauer zu definieren, welche Krebsstadien und Läsionen mit dieser Methode erkannt werden können. Die Auswirkungen reichen weit über Darmkrebs hinaus. Durch die Untersuchung von Unterschieden zwischen Unterarten innerhalb derselben Bakterienart können Forscher beginnen aufzudecken, wie Darmmikroben eine Vielzahl von Gesundheitszuständen beeinflussen. „Die gleiche Methode könnte bald zur Entwicklung nicht-invasiver Diagnosewerkzeuge für eine Vielzahl von Krankheiten genutzt werden, die alle auf einer einzigen Mikrobiota-Analyse basieren“, so Mirko Trajkovski.
Der innovative Ansatz dieser Studie liegt darin, nicht nur grob zwischen Bakterienarten zu unterscheiden, sondern feiner auf Unterarten zu schauen. Diese liefern deutlich präzisere Informationen darüber, welche mikrobiellen Prozesse im Körper ablaufen. So könnten künftig spezifische „Mikrobiom-Profile“ identifiziert werden, die etwa auf Stoffwechselerkrankungen, entzündliche Prozesse oder sogar neurologische Erkrankungen hinweisen. Der große Vorteil: Eine einzige Stuhlprobe könnte ausreichen, um gleichzeitig Hinweise auf verschiedene Gesundheitsrisiken zu liefern.
Langfristig könnte das die medizinische Diagnostik grundlegend verändern. Statt vieler einzelner Tests für unterschiedliche Krankheiten wäre es denkbar, eine umfassende Analyse der Darmmikrobiota als Routineuntersuchung einzusetzen. Ärztinnen und Ärzte könnten dadurch früher eingreifen, Therapien individueller anpassen und Krankheitsverläufe besser überwachen. Noch steht diese Entwicklung am Anfang, aber sie zeigt, wie stark personalisierte Medizin und moderne Datenanalyse – etwa durch maschinelles Lernen – die Vorsorge in Zukunft prägen könnten.