Eine aktuelle Studie berichtet, dass die Verwendung reduzierter Mengen zugelassener Immuntherapeutika bei malignen Melanomen zu einer besseren Kontrolle der Tumore führen und gleichzeitig die Nebenwirkungen begrenzen kann. Die Ergebnisse stammen von Forschern des Karolinska Institutet und wurden im Journal of the National Cancer Institute veröffentlicht. „Die Ergebnisse sind für die Onkologie sehr interessant, da wir zeigen, dass eine niedrigere Dosis eines Immuntherapeutikums nicht nur deutlich weniger Nebenwirkungen verursacht, sondern auch bessere Ergebnisse bei der Bekämpfung von Tumoren und eine längere Überlebenszeit erzielt“, sagt die letzte Autorin Hildur Helgadottir, Forscherin am Institut für Onkologie-Pathologie des Karolinska-Instituts, die die Studie leitete.
Was sind maligne Melanome?
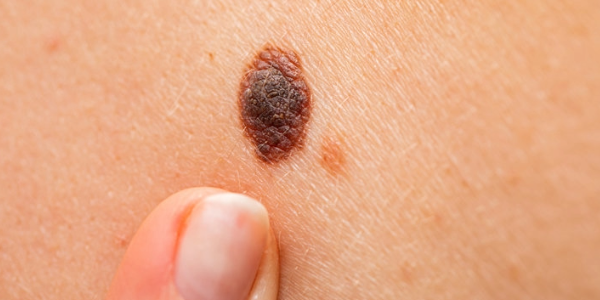
Maligne Melanome sind bösartige Tumoren der pigmentbildenden Zellen (Melanozyten) der Haut. Sie gelten als die gefährlichste Form des Hautkrebses, weil sie schnell wachsen und früh Metastasen in anderen Organen bilden können. Maligne Melanome entstehen häufig aus zuvor unauffälligen Muttermalen, können aber auch neu auftreten. Zu den wichtigsten Risikofaktoren gehören intensive oder wiederholte UV-Strahlung, Sonnenbrände – besonders in der Kindheit –, helle Hauttypen sowie genetische Veranlagung. Eine frühe Erkennung ist entscheidend, da Melanome in frühen Stadien gut behandelbar sind, während fortgeschrittene Melanome eine deutlich schlechtere Prognose haben. Maligne Melanome können grundsätzlich in jedem Alter auftreten, kommen jedoch am häufigsten bei Erwachsenen mittleren bis höheren Alters vor. Typischerweise steigt das Risiko ab etwa dem 40. Lebensjahr deutlich an.
Warum Schweden einen modifizierten Behandlungsansatz verfolgt
Die Standardbehandlung für malignes Melanom im Rahmen der Immuntherapie basiert in der Regel auf den zugelassenen Dosierungen von Nivolumab und Ipilimumab. Da die Kombination in voller Dosierung jedoch häufig zu erheblichen Nebenwirkungen führt, setzen schwedische Ärzte zunehmend auf ein Behandlungsschema mit einer reduzierten Menge an Ipilimumab. Dieser Wirkstoff ist sowohl der teuerste Bestandteil der Behandlung als auch derjenige, der am stärksten mit Nebenwirkungen in Verbindung gebracht wird. „In Schweden haben wir mehr Freiheit bei der Wahl der Dosierung für Patienten, während in vielen anderen Ländern aufgrund der Erstattungsrichtlinien die von den Arzneimittelbehörden zugelassenen Dosierungen vorgeschrieben sind“, sagt Hildur Helgadottir.
Verbesserte Reaktionen und Überlebensrate mit reduzierter Ipilimumab-Dosis
Fast 400 Menschen mit fortgeschrittenem, inoperablem malignen Melanom nahmen an der Studie teil, die sich auf diese schwere Form von Hautkrebs konzentrierte. Den Ergebnissen zufolge zeigten Patienten, die das niedrigere Ipilimumab-Regime erhielten, stärkere Reaktionen. Insgesamt 49 Prozent dieser Patienten sprachen auf die Behandlung an, verglichen mit 37 Prozent in der Gruppe, die die herkömmliche Dosis erhielt.
Das progressionsfreie Überleben, definiert als die Zeit, in der ein Patient ohne Verschlechterung der Krankheit lebt, erreichte in der Gruppe mit niedrigerer Dosis einen Median von neun Monaten. In der Gruppe mit herkömmlicher Dosis lag der Median bei drei Monaten. Auch das Gesamtüberleben unterschied sich signifikant, mit Medianwerten von 42 Monaten bzw. 14 Monaten.
Geringere Nebenwirkungen ermöglichen möglicherweise eine längere Behandlung
Bei 31 Prozent der mit der niedrigeren Dosis behandelten Personen traten schwerwiegende Nebenwirkungen auf, verglichen mit 51 Prozent derjenigen, die die Standarddosis erhielten. „Die neuen Immuntherapien sind sehr wertvoll und wirksam, können aber gleichzeitig schwerwiegende Nebenwirkungen verursachen, die manchmal lebensbedrohlich oder chronisch sind. Unsere Ergebnisse deuten darauf hin, dass diese niedrigere Dosierung es mehr Patienten ermöglichen könnte, die Behandlung über einen längeren Zeitraum fortzusetzen, was wahrscheinlich zu besseren Ergebnissen und einer längeren Überlebenszeit beiträgt“, sagt Hildur Helgadottir.
Obwohl zwischen den Behandlungsgruppen einige Unterschiede bestanden, blieb der Vorteil der niedrigeren Dosierung auch nach Berücksichtigung verschiedener Faktoren, darunter Alter und Tumorstadium, bestehen. Da es sich um eine retrospektive Beobachtungsstudie handelte, kann die Forschung nicht schlüssig beweisen, dass die niedrigere Dosis direkt zu den verbesserten Ergebnissen geführt hat.